Prólogo: en busca de alternativas
Corrían los años cincuenta y la única opción que existía para tratar la ansiedad y el insomnio eran los barbitúricos. Sí, había bromuros, alcohol, opiáceos y alguna sustancia más, pero nada tan efectivo como los barbitúricos.
La molécula original, el ácido barbitúrico, fue descubierta en el año 1867 por el químico alemán Adolf von Baeyer. El origen del nombre de esta molécula aún es un misterio, y existen diferentes hipótesis sobre este. Lo más probable es que el nombre provenga de Santa Bárbara. Parece ser que Baeyer y sus compañeros fueron a celebrar el descubrimiento del ácido barbitúrico a una taberna en la que la artillería del pueblo estaba celebrando Santa Bárbara (la patrona de los artilleros). Otra historia relata que Baeyer obtuvo los precursores necesarios para sintetizar el ácido barbitúrico de la orina de una camarera de Múnich llamada Bárbara. Baeyer juntó el nombre Bárbara y la palabra urea, compuesto presente en la orina necesario para preparar ácido barbitúrico, y así bautizó a su nueva creación.
Sin embargo, no sería hasta el año 1903 cuando el primer barbitúrico con efectos hipnóticos y sedantes sería descubierto. Los científicos Emil Fisher y Josef von Mering crearon el barbital, que rápidamente se patentó y salió al mercado bajo el nombre comercial Veronal®. Una vez más, existen diversas hipótesis sobre el origen de este nombre. Una de ellas dice que, para Mering, Verona era el lugar más pacífico que conocía.
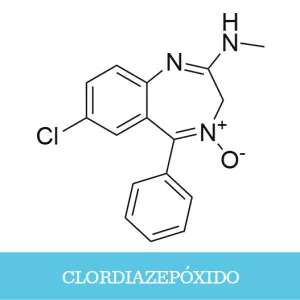
Más tarde irían apareciendo nuevos barbitúricos con acciones diferentes. Los de larga duración, como el fenobarbital (Luminal®) o el ya mencionado barbital (Veronal®), se usaban para tratar las convulsiones. Hoy en día aún se da este uso al fenobarbital. Los de duración intermedia y corta, como el amobarbital (Amytal®) o el pentobarbital (Nembutal®), se empleaban para tratar el insomnio y la ansiedad. Estos han caído en desuso, y es posible que el único lugar en el que entremos en contacto con estos fármacos sea en una novela de Agatha Christie. Finalmente, también se descubrieron los barbitúricos de acción ultracorta, como el tiopentato de sodio, usados para la anestesia. Aún se emplean para esto, pero otros fármacos, como el propofol, están tomando el relevo.
En la década de los cincuenta comenzó a hacerse aparente la necesidad de encontrar nuevas sustancias para tratar patologías tan comunes como la ansiedad o el insomnio. Si bien los barbitúricos eran superiores a los bromuros y otros agentes, su potencial de generar dependencia era muy alto. El síndrome de abstinencia, similar al delirium tremens, podía ser letal. Finalmente, las sobredosis accidentales con estos fármacos iban en aumento, especialmente cuando se mezclaban con otras sustancias que deprimen el sistema nervioso central. Muchas estrellas, como Marilyn Monroe o Jimi Hendrix, sucumbieron al sueño barbitúrico.
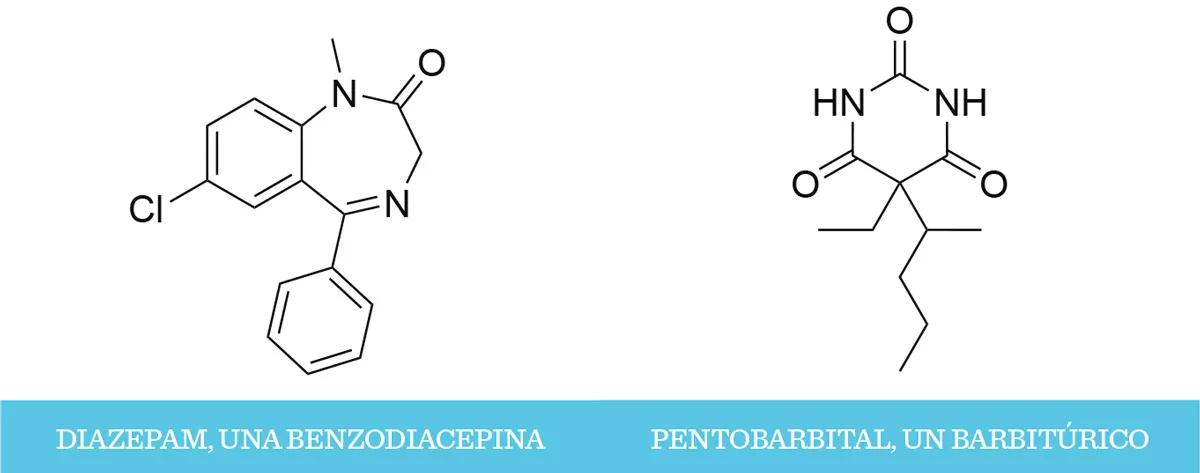
Para el alivio de algunos, comenzaron a aparecer nuevas moléculas que intentarían tomar el testigo, como el meprobamato (Miltown®), la glutetimida (Doriden®) o el etclorvinol (Placidyl®). Sin embargo, fue necesaria la intervención de la serendipia para que irrumpieran las nuevas moléculas que, de una vez y por todas, sustituirían a los barbitúricos: las benzodiacepinas.
Capítulo I: un golpe de suerte
Leo Henryk Sternbach era una persona desordenada pero tozuda. Un químico polaco que obtuvo su título de doctor en el año 1931 en Cracovia, y al principio de su carrera se centró en tintes y colorantes. Sin embargo, sobrevino la segunda guerra mundial y optó por huir a Estados Unidos. En el año 1954 se encontraba trabajando en Nueva Jersey para Hoffmann-La Roche, un mastodonte farmacéutico que se había obcecado en encontrar nuevos sedantes y tranquilizantes. Sternbach, acordándose de su trabajo con tintes, pensó que sería interesante modificar la estructura química de los compuestos que había sintetizado para intentar obtener nuevos fármacos. ¿La razón? La reciente comercialización de la clorpromazina, el primer antipsicótico, que presentaba cierta similitud química con sus compuestos.
Con la ayuda de sus compañeros, Sternbach sintetizó decenas de derivados, ninguno de los cuales dio resultados favorables en los ensayos. Para colmo, poco después, el grupo liderado por el químico polaco se dio cuenta de que la estructura de los compuestos que estaba sintetizando no tenía nada que ver con la esperada. Los fracasos se fueron apilando y, a mediados del año 1955, los esfuerzos del grupo fueron redirigidos a los antibióticos, dejando de lado los hipnosedantes. Mas esta nueva vía de investigación también resultó fútil y, hacia el año 1957, las frustraciones se habían acumulado considerablemente, al igual que el desorden en el laboratorio. Solo había una opción: limpiar el caos imperante en las instalaciones y empezar de cero. Fue en este momento cuando un compañero de Sternbach, Earl Reeder, se topó con un bello sólido cristalino que había sido sintetizado hacía dos años, pero nunca pudo ser estudiado en ensayos biológicos debido a varios contratiempos. Estaban seguros de que el compuesto no sería activo, pero igualmente lo enviaron a los farmacólogos para que lo estudiasen. Qué sorpresa recibieron cuando, en mayo de 1957, el farmacólogo Lowell O. Randall les llamó para informarles de que el compuesto era altamente activo. Su técnica de laboratorio, la habilidosa y observadora Beryl Kappell, quien había hecho ensayos con los compuestos que habían ido sintetizando Sternbach y sus colegas, estudió el bello sólido cristalino, y se quedó atónita al ver que presentaba las propiedades deseadas.
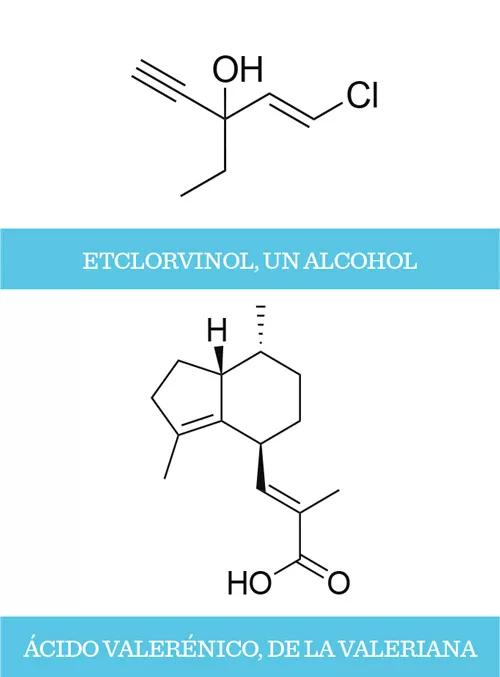
Pronto Sternbach se daría cuenta de que la molécula en cuestión presentaba una estructura química totalmente diferente a la que le había asignado. Resultó ser una benzodiacepina, a la que llamó clordiazepóxido. Después de tres años de estudios, en el año 1960, este compuesto se comercializó bajo el nombre de Librium®. Le seguirían decenas de benzodiacepinas, muchas de ellas sintetizadas por el propio Sternbach, como el diazepam (Valium®), el clonazepam (Klonopin®) y el flunitrazepam (Rohypnol®).
Estas moléculas presentaban un perfil de seguridad mucho más alto que los barbitúricos. Por fin, después de años de plegarias, la serendipia había actuado. Los barbitúricos eran algo del pasado, y las benzodiacepinas tomarían las riendas.
A día de hoy, y más de sesenta años desde su descubrimiento, siguen siendo los hipnosedantes por excelencia. Son recetados para tratar todo tipo de trastornos, a veces, con demasiada facilidad. Y es que, a pesar de ser mucho más seguras que los barbitúricos, las benzodiacepinas también presentan potencial para generar dependencia. Sin embargo, cada año se producen y distribuyen toneladas de estas sustancias. A modo de ejemplo, España calcula que este año necesitará dos toneladas de lorazepam. Asumiendo que la dosis de lorazepam es un miligramo, esto equivale a la friolera de dos mil millones de dosis.
Capítulo II: potenciando el GABA
Hoy en día sería impensable, pero, cuando en 1960 se sacó al mercado el clordiazepóxido, no se tenía ni idea de cómo funcionaba esta molécula en el cerebro. Habría que esperar a los años setenta para que diversos grupos de investigadores se pusieran de acuerdo en que estos fármacos afectan a un neurotransmisor llamado GABA.
El ácido gamma-aminobutírico, GABA para los amigos, es el principal neurotransmisor depresor de nuestros cerebros. Se une a diversos receptores y hace que nuestro sistema nervioso se ralentice. Entre los receptores a los que afecta este neurotransmisor, se observó que las benzodiacepinas mostraban preferencia por el receptor GABAA. Este es, esencialmente, un canal que permite el paso al interior de la neurona aniones (átomos cargados negativamente); más específicamente, aniones cloruro (derivados del cloro). Cuando el GABA se une a este receptor, el canal se abre, dejando pasar al anión cloruro. Algo que parece tan baladí genera una diferencia de cargas entre el exterior y el interior de la neurona, y provoca, después de una serie de mecanismos, la depresión del sistema nervioso.
Este canal, el receptor GABAA, tiene diferentes bolsillos por su superficie. A uno de ellos se une el GABA, mientras que al resto, no, pero sí se pueden unir otras variopintas moléculas. ¿Cuáles? Aquí es donde entran en juego las benzodiacepinas. Sí, las benzodiacepinas ocupan estos bolsillos, modulando la actividad del GABA a distancia (la palabra técnica es modulación alostérica). Esencialmente, al ocupar esos bolsillos, lo que están causando las benzodiacepinas es que el GABA sea más activo cuando se une al receptor. De alguna manera, es parecido a un control remoto pero a nivel molecular. A nivel bioquímico, lo que ocurre es que el canal que permite el paso de aniones se abra con más frecuencia cuando hay una benzodiacepina unida a esos bolsillos.
Pero hay muchos más bolsillos en el receptor GABAA, y una gran variedad de sustancias depresoras se unen a estos. Los vetustos barbitúricos, el omnipresente alcohol o la apestosa valeriana presentan una actividad similar, solo que se unen a otros bolsillos. Esto explicaría por qué los efectos de una benzodiacepina y del alcohol son distintos, si bien los dos son depresores. Gracias a esta abundancia de bolsillos, moléculas que no presentan ninguna similitud estructural modulan este receptor. Y es que incluso el mismo bolsillo puede ser la diana de moléculas muy dispares. Por ejemplo, el ácido valerénico, que se considera el componente activo de la valeriana, interactúa con el mismo bolsillo con el que interactúan la metacualona, antiguo hipnosedante que se distribuyó bajo el nombre comercial de Quaalude®, y el etomidato, un anestésico general.
Vista toda esta farmacología, más de un investigador se preguntó qué sucedería si, en vez de emplear una molécula que funciona a distancia, se creasen fármacos que directamente abrieran el canal, como hace el GABA. Pues bien, estas moléculas existen, pero cuando penetran en el cerebro humano y ejercen su actividad comienzan a suceder cosas raras. ¿Algún ejemplo? El muscimol, el principio activo de la Amanita muscaria. Resulta que la activación directa del receptor GABAA por moléculas exógenas (foráneas a nuestro cuerpo) produce, más allá de sedación, alucinaciones y extrañas distorsiones. Estos compuestos se están estudiando, pero parece que no serán los nuevos hipnosedantes que sustituyan a las benzodiacepinas.
Capítulo III: nuevas benzodiacepinas en el horizonte

El siglo xxi ha traído aires renovados al mundo de las drogas. Las nuevas sustancias psicoactivas (comúnmente denominadas NPS, siglas del nombre en inglés: new psychoactive substances) han inundado las redes, y análogos legales (o, mejor dicho, alegales) han aparecido como sustitutos a las sustancias clásicas. Fenetilaminas, catinonas y cannabinoides son posiblemente las familias químicas más nombradas. Pero también hay un nicho reservado para las benzodiacepinas. Muchas de las nuevas benzodiacepinas que se están vendiendo no tienen nada de nuevas. Son compuestos que se sintetizaron en los mismos laboratorios donde nacieron el alprazolam o el lorazepam, pero no corrieron la misma suerte. Fueron olvidados, hasta que la era de las NPS los desenterró.
La mayoría de estas nuevas benzodiacepinas presentan similitud con nuestras viejas conocidas, así como una actividad parecida. Su perfil de seguridad no está del todo establecido, por lo que siempre hay que actuar con cautela. Y como son productos que no han pasado ningún control de calidad, es esencial analizarlas.
Hay diversas razones por las que se obtienen estas nuevas benzodiacepinas: uso recreativo, automedicarse cuando no es posible el acceso a benzodiacepinas aprobadas, experimentación, entre otras. Y también están apareciendo como adulterantes en otras benzodiacepinas.
Desde el año 2010, se han analizado en Energy Control un total de 638 muestras de benzodiacepinas. Con diferencia, la sustancia más analizada ha sido el alprazolam, pues se han analizado un total de 389 muestras del mismo. Pues bien, de todas ellas, resulta que solo el cincuenta por ciento contenían alprazolam, y casi un ocho por ciento contenían etizolam, una benzodiacepina que hasta el 2020 se vendió por internet, año en el que se fiscalizó.
Y si nos centramos en los últimos cuatro años, solo un veinticinco por ciento de las muestras de alprazolam contenían la sustancia deseada. Por otro lado, más del veinte por ciento contenían otra nueva benzodiacepina, el bromazolam; esta sustancia es estructuralmente muy semejante al alprazolam, pero no se encuentra regulada como psicótropo. Como ha anunciado la International Narcotics Control Board (INCB), esto cambiará a finales de este año, cuando el bromazolam sea fiscalizado e incluido en la Lista IV del Convenio sobre Sustancias Sicotrópicas de 1971, junto con el resto de benzodiacepinas. Pero no debemos preocuparnos, pues hay otras decenas de moléculas ansiosas de ocupar su lugar.
Antes de cerrar este capítulo, sería importante hablar de NPS derivadas de otras sustancias depresoras. En el caso de los barbitúricos, parece que su capítulo en la historia se ha cerrado para siempre. Esporádicamente han aparecido nuevos derivados de barbitúricos, pero esto ha sido raro. Sin embargo, casi una decena de análogos de la metacualona han emergido, muchos de ellos muy peligrosos. Derivados como la metilmetacualona provocan convulsiones a dosis solo ligeramente superiores a la dosis recreativa. Otro análogo, el SL-164, no solo provoca estas convulsiones, sino que además se ha encontrado tiznado con un precursor que puede provocar cáncer de vejiga. Al igual que con los barbitúricos, parece ser que la era de la metacualona finalizó en los años ochenta.
Epílogo: el ocaso de las benzodiacepinas
Tal y como pasó con los barbitúricos hace más de sesenta años, a día de hoy se están buscando nuevas moléculas que sustituyan a las benzodiacepinas. Son mucho más seguras, pero siguen presentando problemas de dependencia, y a edades avanzadas los efectos adversos son más notables.
Unos nuevos fármacos muy prometedores son los antagonistas de los receptores de orexina. A diferencia de las benzodiacepinas, estas moléculas no actúan sobre el GABA. Lo que hacen es bloquear los receptores de orexina, que regulan la vigilia y el sueño. En el año 2022 se aprobó el primer fármaco de esta familia en la Unión Europea, conocido como daridorexant. Otros, como el lemborexant o el suvorexant, también están comercializados en Estados Unidos. Asimismo, diversas sustancias como los antihistamínicos, la melatonina y sus derivados, cannabinoides y antidepresivos, entre otras, se están empleando como sustitutos, pero sin el éxito desbordante que muestran las benzodiacepinas.
Quién sabe, igual, en algún laboratorio caótico, está esperando una bella sustancia cristalina a que la diosa Fortuna le sonría para poder convertirse en la nueva estrella de los hipnosedantes, y así cerrar para siempre jamás el reinado de las benzodiacepinas.